
















Ատոմի միջուկի շուրջը գտնվող էլեկտրոնների համախումբը առաջացնում է էլեկտրոնային թաղանթը:
Էլեկտրոնների թիվը ատոմի էլեկտրոնային թաղանթում հավասար է ատոմի միջուկում պրոտոնների թվին, որը որոշվում է Մենդելեևի պարբերական համակարգում տարրի կարգաթվով կամ ատոմային համարով:
Այսպես, ջրածնի ատոմի էլեկտրոնային թաղանթը կազմված է մեկ էլեկտրոնից, կալցիումինը՝ \(20\), արծաթինը՝ \(47\):
Իսկ ինչպե՞ս են շարժվում էլեկտրոնները: Քաոսայի՞ն, վառվող լամպի շուրջը պտտվող մժեղների նմա՞ն, թե՞ որոշակի կարգավորվածությամբ: Այդ հարցի պատասխանը կարելի է գտնել՝ դիտարկելով էլեկտրոնի էներգիական բնութագիրը:
Էլեկտրոններն ատոմում տարբերվում են իրենց էներգիայով: Ինչպես ցույց են տալիս փորձնական արդյունքները, որոշ էլեկտրոններ ավելի ուժեղ են ձգվում միջուկի կողմից, մյուսները՝ ավելի թույլ: Այս երևույթի գլխավոր պատճառը էլեկտրոնների տարբեր հեռավորությունն է ատոմի միջուկից:
Ինչքան էլեկտրոնները մոտ են ատոմի միջուկին, այնքան ավելի ամուր են կապված և նրանց դժվար է պոկել էլեկտրոնային թաղանթներից, իսկ ինչքան էլեկտրոնները հեռու են միջուկից, այնքան նրանց հեշտ է պոկել:
Միջուկին առավել մոտ պտտվող էլեկտրոնները կարծես թե շրջափակում են միջուկը մյուս էլեկտրոններից, որոնք միջուկի կողմից ավելի թույլ են ձգվում, և հետզհետե հեռավորությունը միջուկից մեծանում է: Այսպես են առաջանում էլեկտրոնային շերտերնատոմի էլեկտրոնային թաղանթում:
Ատոմի էլեկտրոնային թաղանթում էլեկտրոնները բաշխված են էլեկտրոնային շերտերի ձևով:
Առաջինը միջուկին մոտ գտնվող էլեկտրոնային շերտն է, որում էլեկտրոնն օժտված է նվազագույն էներգիայով: Վերջին՝ միջուկից ամենահեռու գտնվող էլեկտրոնային շերտն անվանվում է արտաքին:
Ատոմի այդ վիճակն անվանում են հիմնական վիճակ:
Յուրաքանչյուր էլեկտրոնային շերտում գտնվում են էներգիայի արժեքով միմյանց մոտ էլեկտրոններ: Այդ պատճառով էլ էլեկտրոնային շերտն անվանվում է նաև էներգիական մակարդակ:
Էներգիական մակարդակների թիվը քիմիական տարրի ատոմում հավասար է պարբերական աղյուսակում այդ տարրի պարբերության համարին:
Օրինակ
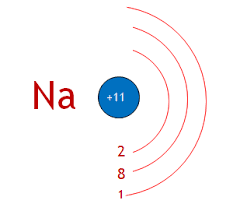
Նատրիումը գտնվում է \(3\)-րդ պարբերությունում հետևաբար ատոմում առկա \(11\) էլեկտրոնները բաշխված են երեք էներգիական մակարդակներում:
Տվյալ էներգիական մակարդակում գտնվող էլեկտրորրերի առավելագույն թիվը որոշվում է բանաձևով, որտեղ \(n\)-ը մակարդակի համարն է:
Առաջին էլեկտրոնային շերտում երկուսից ավելի էլեկտրոն չի կարող լինել:
Ցանկացած ատոմի արտաքին էլեկտրոնային շերտում (բացառությամբ որոշ տարրերի ատոմների) էլեկտրոնների թիվը չի կարող \(8\)-ից մեծ լինել:
Էլեկտրոնների թիվը գլխավոր ենթախմբերի տարրերի արտաքին էներգիական մակարդակում հավասար է խմբի համարին:
Գրառումը, որն արտացոլում է քիմիական տարրի ատոմում էլեկտրոնների բաշխումն ըստ էներգիական մակարդակների և ենթամակարդակների, կոչվում է այդ ատոմի էլեկտրոնային փոխդասավորվածություն (էլեկտրոնային բանաձև):
Օրինակ
Նատրիում տարրի ատոմի էլեկտրոնային բանաձևն է ` :