
















Քլոր՝ պարզ նյութ: Քլորի ստացումը:


Բնական քլորը երկու իզոտոպի խառնուրդ է` \( (\)\(75,5\)%\()\) և \((\)\(24,5\)%\():\)
Քլոր տարրի հարաբերական ատոմային զանգվածը որոշվում է հետևյալ ձևով.
Սովորական պայմաններում քլորը սուր, հեղձուցիչ հոտով դեղնականաչավուն գազ է: Սենյակային ջերմաստիճանում \(1\) ծավալ ջրում \(2,5\) ծավալ քլոր է լուծվում, առաջացնելով դեղնավուն լուծույթ՝ քլորաջուր:

Գազային քլոր

Քլորաջուր
Գազային քլորը մոտ \(0,6\) ՄՊա ճնշման տակ, սենյակային ջերմաստիճանում վերածվում է հեղուկի:
Հեղուկ քլորը պահում են և փոխադրում եմ պողպատե տարաներում:

Հեղուկ քլորի տարաները
Ե՛վ արդյունաբերության մեջ, և՛ լաբորատորիայում քլոր ստանում են քլորիդ \((\)\()\) իոնների օքսիդացումից՝
Լաբորատորիայում քլոր ստանում են հիմնականում աղաթթվի ու մանգանի\((IV)\) օքսիդի փոխազդեցությունից՝
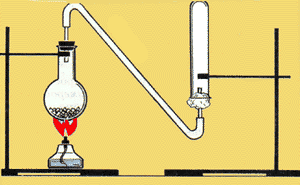
Քլորի ստացման սարք
Որպես օքսիդացնող նյութ կարելի է վերցնել նաև՝ և այլն:
Արդյունաբերության մեջ քլոր ստանում են նատրիումի քլորիդի հալույթի կամ խիտ ջրային լուծույթի միջով հաստատուն էլեկտրական հոսանք անցկացնելով (էլեկտրոլիզից):

Նատրիումի քլորիդի ջրային լուծույթի
էլեկտրոլիզ
Յուրաքանչյուր տարրի աշխարհում արտադրվում է մոտ \(30\) մլն տոննա քլոր:
Աղբյուրները
Ա.Սահակյան և ուրիշներ, քիմիա 9, Երևան 2015