
















Ատոմի կառուցվածքի վերաբերյալ տեսակետների զարգացումը
Նյութի մանրացման աստիճանի, կամ բաժանելիության սահմանի մասին առաջին դատողություններն արվել են Հույն փիլիսոփա Դեմոկրիտոսի (մ.թ.ա. \(460-370\) թ.) կողմից: Նա ենթադրում էր, որ նյութի փոքրագույն մասնիկը ատոմն է, որը թարգմանաբար նշանակում է անբաժանելի:


Մոտ երկու հազար տարի անց անգլիացի քիմիկոս Ջ. Դալթոնը զարգացրեց նյութի կառուցվածքի ատոմիստական տեսությունը (\(1803\) թ.), ըստ որի բոլոր պարզ նյութերը բաղկացած են գնդաձև անբաժանելի ատոմներից:

Ջոն Դալթոն
Սակայն \(19\)-րդ դարի ընթացքում բացահայտվեցին մի շարք երևույթներ, որոնք խարխլեցին ատոմի անբաժանելիության մասին կարծիքը: Ահա դրանցից մի քանիսը`
* Էլեկտրական հոսանքի անցումը էլեկտրոլիտների ջրային լուծույթներում (Մ. ֆարադեյ, \(1833\) թ):
* Էլեկտրական հոսանքի անցումը նոսրացված գազերում, էլեկտրոդների միջև բարձր լարում կիրառելիս (կաթոդային ճառագայթներ, \(1870\) թ):
* Բնական ռադիոակտիվության հայտնագործումը ֆրանսիացի ֆիզիկոս Ա. Բեքերելի կողից (\(1896\) թ.):
* Էլեկտրոնի հարաբերական լիցքի և զանգվածի որոշումը գիտափորձերով անգլիացի ֆիզիկոս Ջ. Թոմսոնի կողմից (\(1897\) թ) և այլն:
Ատոմի բարդ մասնիկ լինելը, արդեն, կասկածից վեր էր, մնում էր բացահայտել նրա կառուցվածքը:
Ատոմի կառուցվածքի առաջին մոդելը տվել է անգլիացի ֆիզիկոս Ջ. Թոմսոնը (\(1904\) թ.).
Ատոմի կառուցվածքի Թոմսոնի մոդելը աշխարհին հայտնի է «պուդինգ», «չամչով կեքս», կամ «չամչով փլավ» անուններով, ըստ որի բացասական լիցք ունեցող էլեկտրոնները համաչափ բաշխված են դրական լիցք ունեցող միջավայրում:
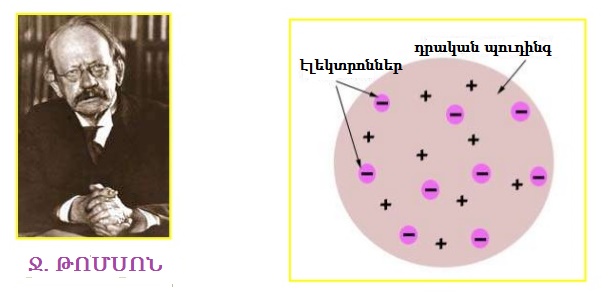
Ակնհայտ է, որ ատոմի կառուցվածքի Թոմսոնի մոդելը մեծ թերություններ ուներ:
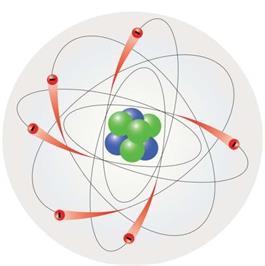
\(1911\) թվին անգլիացի ֆիզիկոս Է. Ռեզերֆորդը հանճարեղ մի գիտափորձով ցույց տվեց, որ ատոմն ունի միջուկային կառուցվածք: Ըստ այդ մոդելի ատոմի միջուկն ունի դրական լիցք, ատոմի գրեթե ողջ զանգվածը կենտրոնացած է միջուկում, միջուկն ունի անհամեմատ փոքր ծավալ ատոմի ծավալի նկատմամբ, իսկ բացասական լիցքավորված էլեկտրոնները գտնվում են միջուկաշուրջ տիրույթում:


Ռեզերֆորդի փորձի էությունը հետևյալն է. ոսկուց պատրաստված շատ բարակ թիթեղը ալֆա-մասնիկներով «ռմբակոծելիս» դրանց մեծ մասն անարգել անցնում է ոսկու թիթեղի միջով, շատ փոքր մասը շեղվում է ուղղագիծ ընթացքից, իսկ միայն չնչին մասը՝ մոտ \(100000\)-ից մեկը, կտրուկ հետ է դառնում:

Է. Ռեզերֆորդ
Ատոմի կառուցվածքի միջուկային մոդելը նույնպես զերծ չէր թերություններից: Oրինակ` ինչպե՞ս էլեկտրոնները չեն ընկնում միջուկի վրա:
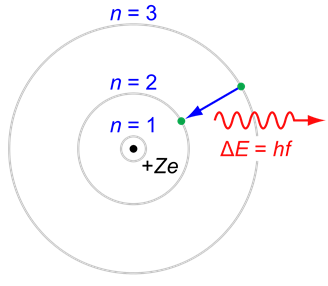
Շատ կարճ ժամանակ անց` \(1913\) թվին, Ն. Բորը առաջարկեց ատոմի կառուցվածքի մոլորակային մոդելը, ըստ որի էլեկտրոնները պտտվում են միջուկի շուրջը շրջանաձև ուղեծրով՝ օրբիտաներով, ինչպես մոլորակներն Արևի շուրջը:

Ն. ԲՈՐ
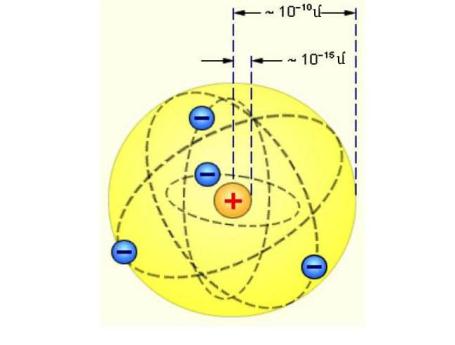
Բորը հաշվարկեց ջրածնի էլեկտրոնի շարժման ուղեծրի շառավիղը, այսինքն ջրածնի ատոմի շառավիղը, հաստատեց Ռեզերֆորդի փորձի արդյունքները ատոմի և ատոմի միջուկի չափսերի վերաբերյալ: Ինչպես երևում է ստորև բերված նկարում միջուկի չափսը մոտ \(100000\) անգամ փոքր է ատոմի չափսից:
Ատոմի կառուցվածքի վերաբերյալ տեսակետների հետագա զարգացումը առնչվում է գիտության, տեխնիկայի և ինժեներական մտքի հետագա զանգացման, նոր, ժամանակակից տեսությունների ստեղծման, մասնավորապես, հարաբերականության տեսության և էլեկտրոնի երկվության՝ էլեկտրոնի ալիքամասնիկային հատկությունների հայտնաբերման, քվանտային մեխանիկայի նվաճումների հետ:
Ստորև բերված նկարում կարող ենք տեսնել ատոմի կառուցվածքի վերաբերյալ տեսակետների զարգացման ժամանակագրությունը:
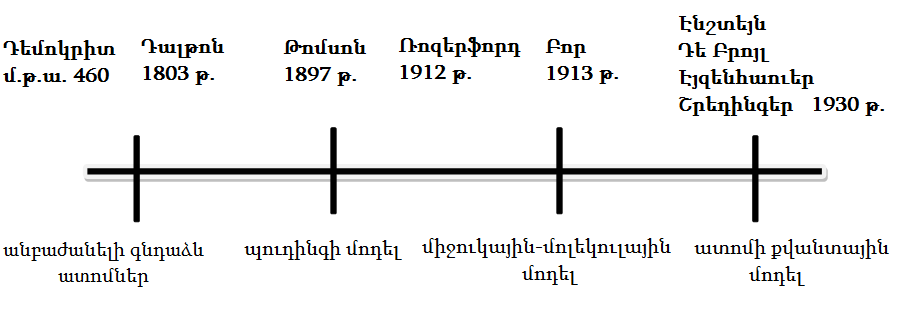
Ատոմի կառուցվածքի պարզաբանման գործում մեծ նվաճումների համար շատ գիտնականեր արժանացել են ՆՈԲԵԼՅԱՆ մրցանակի: Oրինակ`
Ա. Բեքերել - \(1903\) թ. - բնական ռադիոակտիվության հայտնաբերման համար
Ջ. Թոմսոն - \(1906\) թ. - գազերում էլեկտրական հոսանքի անցումը ուսումնասիրելու համար
Ա.Էյնշտեյն - \(1921\) թ. - ֆոտոէլեկտրական էֆեկտի հայտնաբերման համար
Դե. Բրոյլ - \(1929\) թ. - էլեկտրոնի ալիքամասնիկային երկակի բնույթի հայտնաբերման համար
Ջ. Չեդվիգ - \(1935\) թ. - նեյտրոնի հայտնաբերման համար, և ուրիշներ:
Աղբյուրները
Ա․ ԽԱՉԱՏՐՅԱՆ, Լ․ ՍԱՀԱԿՅԱՆ
Քիմիա-10, Երևան-2010